Vår forskning
Vårt laboratorium har två huvudsakliga forskningslinjer: 1) mekanismer för cellödesbeslut i humorala immunsvar och 2) biologi av medfödda liknande lymfocyter. För att lära dig mer om några av våra projekt, titta på vårt senaste Global ImmunoTalks-seminarium:
Mekanismer för cellödesbeslut i humorala immunsvar som ligger till grund för bildandet av immunologiskt minne.
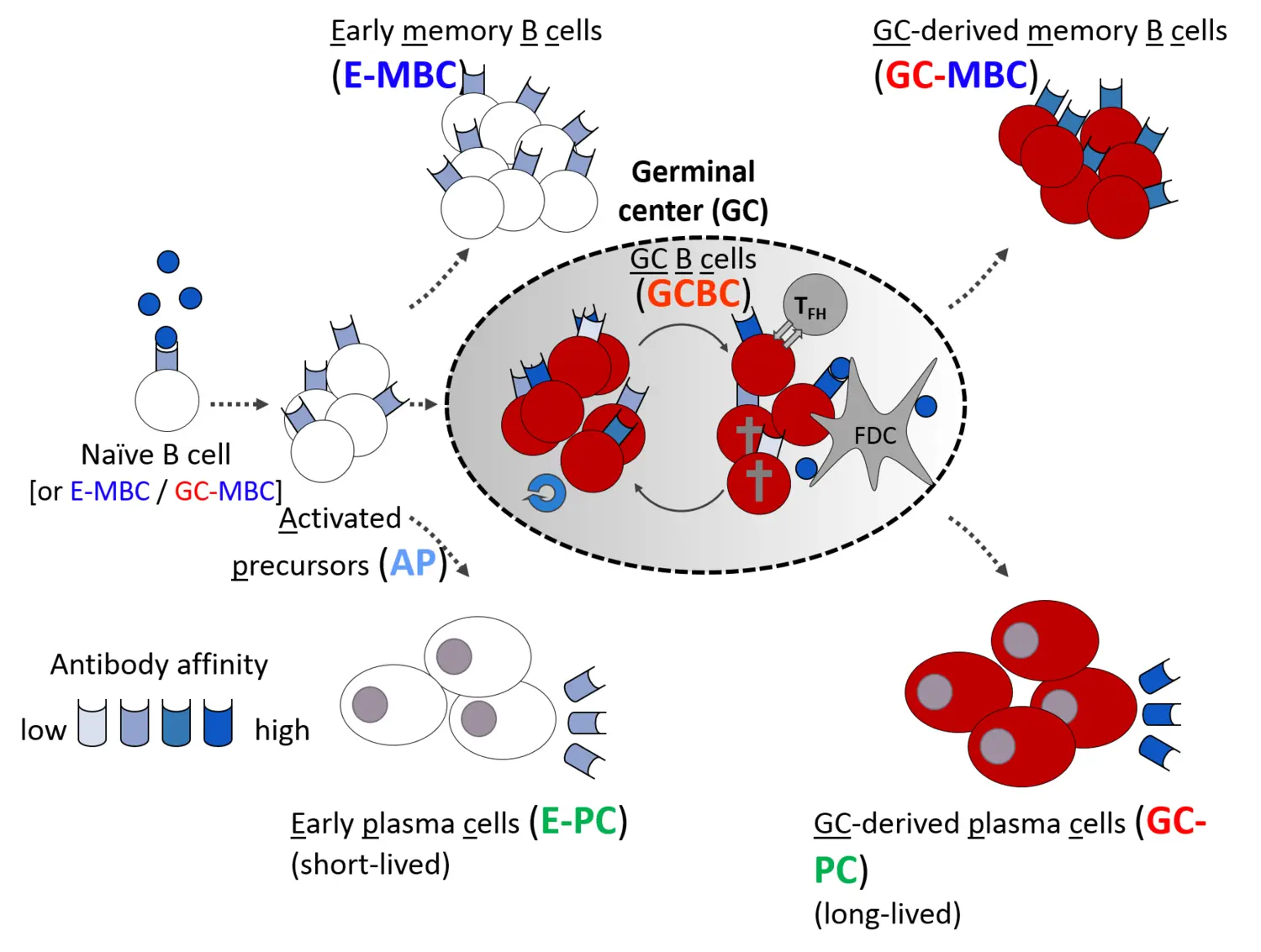
Antigenberoende B-cellsdifferentiering är en ovanlig utvecklingsprocess, där de två huvudsakliga resultaten av det humorala immunsvaret – antikroppsutsöndrande plasmaceller och vilande minnes-B-celler – kan genereras genom två olika vägar: antingen direkt från tidigt aktiverade B-celler, eller efter övergång genom ett transkriptionellt distinkt germinalcenter (GC) B-cellstillstånd.
För att lära dig mer om våra huvudsakliga forskningsområden, titta på vårt Global ImmunoTalks-seminarium “I. Lageridentitet hos B-cellsminne. II. Ovanliga specificiteter hos γδTCRs”.
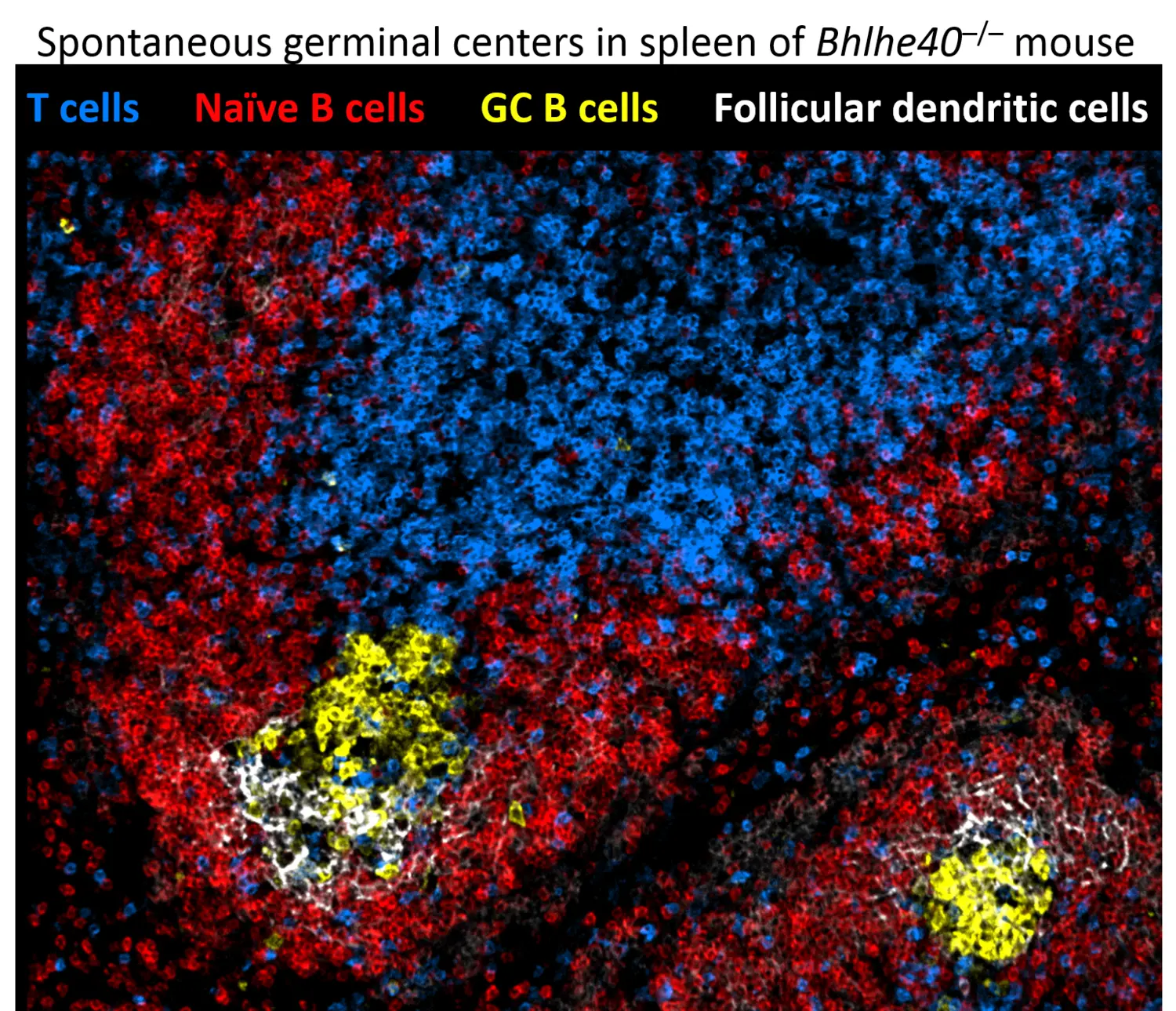
Den första vägen kan generera antikroppsutsöndrande celler mycket snabbt, vilket ger det första försvaret mot patogener. Deltagande i GC-reaktionen tillåter att öka affiniteten hos antikroppar men tar längre tid. Att förstå dessa utvecklingsvägar är av avgörande betydelse, eftersom kvaliteten på immunologiskt minne kan variera kraftigt efter infektion och vaccination, vilket resulterar i olika grad av skydd under den efterföljande mikrobiella utmaningen. Vi undersöker cellulära och molekylära mekanismer som styr bildandet av dessa distinkta vågor av minnes-B-celler och plasmaceller samt deras funktionella egenskaper. I strävan efter detta mål har vi nyligen upptäckt cellintrinsiska funktioner hos transkriptionsfaktorn Bhlhe40 i både B- och T-lymfocytundergrupper involverade i GC-reaktionen (Rauschmeier et al, J Exp Med, 2022). Dessutom avslöjade vårt senaste arbete också att en stor del av aktiverade B-lymfocyter under de första dagarna av svaret genomgår 'differentiering som standard' till germinalcenter-oberoende minnes-B-celler, en population som ofta betraktades som en mindre, obetydlig undergrupp av B-cellsminne (Glaros et al, Immunity, 2021). Dessa oväntade observationer förändrar vår syn på sammansättningen av den långsiktiga B-cellsminnespoolen och öppnar många nya frågor om bildandet av immunologiskt minne mot infektioner och vacciner som vårt laboratorium för närvarande undersöker.
Biologi för medfödda liknande lymfocyter.
Lymfocyter i det adaptiva immunsystemet kan funktionellt delas in i två huvudgrupper. Konventionella T- och B-celler kännetecknas av extremt breda antigenreceptorrepertoarer och kan därför svara på en mängd olika antigener, men deras aktivering, expansion och differentiering till effektorceller kräver flera dagar. Däremot uppvisar medfödda liknande B- och T-celler (t.ex. B1-celler, iNKT-celler och många γδT-cellundergrupper) mer fokuserade antigenreceptorrepertoarer och hålls i ett konstant föraktiverat tillstånd. Dessa celler tros utgöra den första försvarslinjen mot patogener och/eller spela en roll i vävnadshomeostas och reparation. Medan vi har en ganska god förståelse för de biologiska funktionerna, antigenspecificiteterna, selektionsreglerna och transkriptionsprogrammen för de flesta konventionella undergrupper, är detta inte fallet för majoriteten av medfödda liknande populationer. Många grundläggande frågor som för konventionella lymfocyter löstes för år eller till och med årtionden sedan förblir obesvarade för dessa icke-konventionella undergrupper.
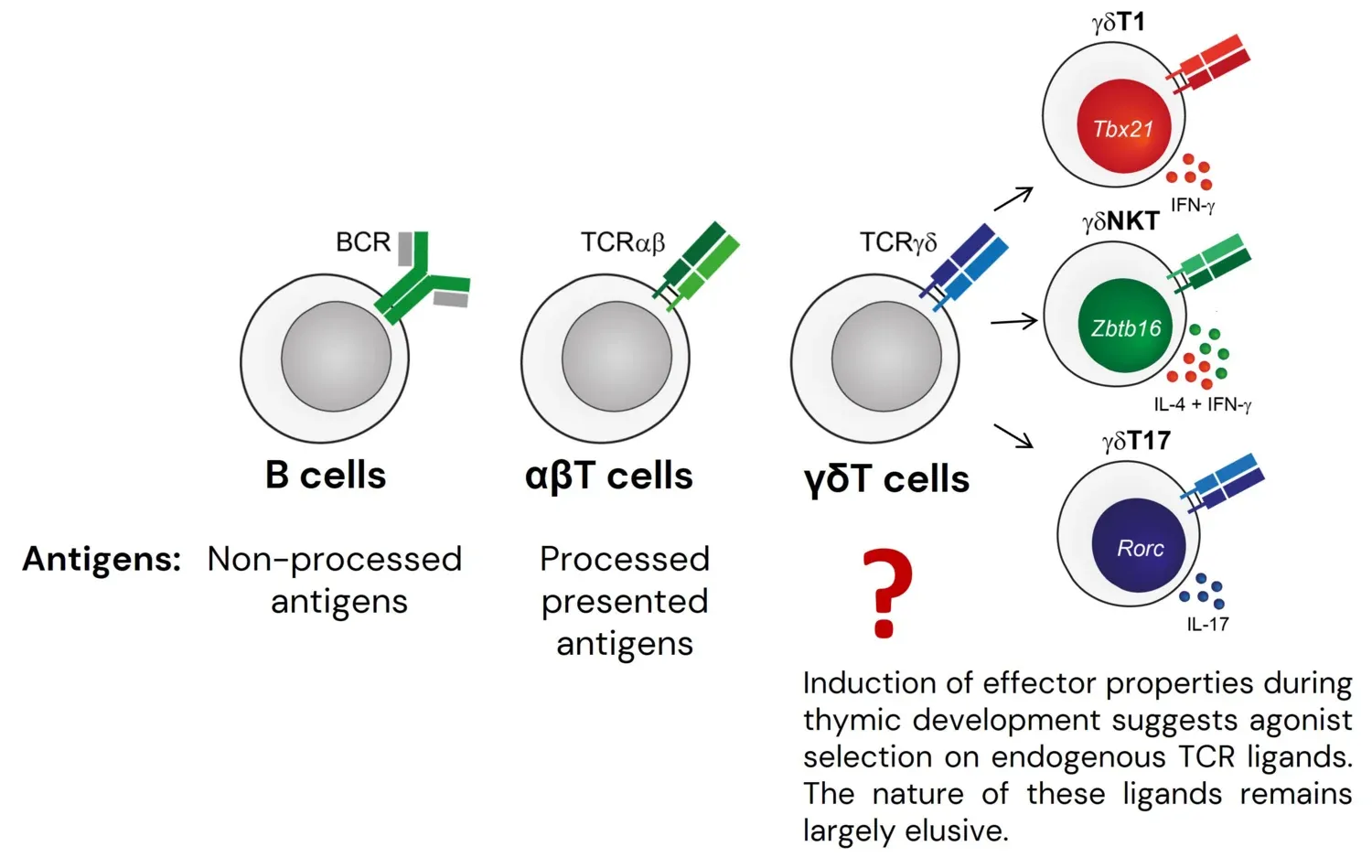
Av de tre typerna av lymfocyter som utgör det adaptiva immunsystemet hos käkförsedda ryggradsdjur är γδT-celler – en population som är särskilt rik på celler med medfödda liknande egenskaper – den enda celltypen för vilken vi inte förstår principerna för antigenigenkänning och vet mycket lite om naturen hos dessa antigener. Det tros att många γδT-celler genomgår agonistisk selektion på endogena ligander, vilket resulterar i förvärv av medfödda liknande effektoregenskaper. I linje med agonistisk selektion av γδT-celler visar våra resultat att en stor del av γδT-celler känner igen en mångfald av okända självantigener. Anmärkningsvärt nog visade vi att majoriteten av dessa antigener inte tillhör kända familjer av γδTCR-ligander, vilket indikerar att de kända endogena γδTCR-liganderna bara representerar toppen av isberget, och att många medfödda liknande γδT-celler sannolikt genomgår agonistisk selektion på en mångfald av oidentifierade molekyler som inte tillhör kända familjer av γδTCR-ligander. Detta resultat belyser hur lite vi förstår om biologin hos dessa celler. För att börja fylla denna kunskapslucka etablerade vi en screeningpipeline som redan har tillåtit oss att identifiera flera nya kandidater för γδTCR-ligander. Vi utforskar nu de funktionella konsekvenserna av denna igenkänning i in vivo-modeller. Den pipeline för ligandidentifiering som vi har etablerat bör tillåta oss att hitta γδTCR-ligander i en mängd olika fysiologiska och patologiska sammanhang och vi tillämpar för närvarande vårt tillvägagångssätt för att identifiera antigener för γδTILs i mänskliga cancerformer.
Utöver vårt intresse för antigenreceptorspecificiteter hos medfödda liknande T-celler är vi också intresserade av deras funktioner. Det har nyligen visats att många medfödda liknande T-celler i thymus representerar vävnadsresidenta celler snarare än nyutvecklade celler som är på väg att lämna till periferin. Anledningarna till ansamlingen av effektor-T-celler på platsen för T-cellsutveckling, där patogenmöten är osannolika, förblev oklara. Vi har visat att thymus medfödda liknande T-celler, en population som uttrycker molekyler som är karakteristiska för alla större aktiverade T-cellundergrupper, kan inducera mycket effektiv CD8 T-cellstolerans mot inflammationsassocierade självantigener, en klass av självantigener som i periferin till stor del speglar den rumsliga och tidsmässiga fördelningen av patogenhärledda molekyler (You et al, Nat Immunol, 2024). Eftersom thymus hyser ett komplext konstitutivt aktivt inflammatoriskt nätverk, med thymus-residenta medfödda liknande T-celler som representerar en av dess centrala noder, tyder dessa resultat på att denna konstitutiva uttryck av inflammationsassocierade molekyler i thymus kan ha utvecklats för att säkerställa induktionen av tolerans mot denna unika klass av självantigener.

