Vår forskning
Fetma och dess associerade sjukdomar fortsätter att öka världen över i en alarmerande takt, med allvarliga socioekonomiska konsekvenser. En djupare förståelse för varför övernäring leder till sjukdomsutveckling behövs snarast, så att förbättrade terapeutiska och förebyggande behandlingar kan utvecklas.
Vår grupp studerar olika aspekter av näringsämneshantering, upptag och lagring hos människor, med särskilt fokus på lipidhantering i fettvävnaden, makrofager och levern. Det övergripande målet är att använda translationella metoder för att belysa signalvägar som, när de störs, bidrar till utvecklingen av kardiometabol sjukdom, med särskilt fokus på ateroskleros och typ 2-diabetes. Vår forskning följer tre huvudlinjer.
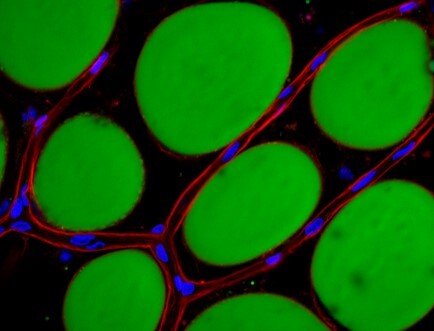
Docent Carolina Hagbergs team studerar lipidhanteringen hos vårt största fettlagringsorgan, den vita fettvävnaden. En stor del av arbetet fokuserar på mikrovaskulaturens avgörande roll för fettvävnadens lipidupptag och expansion, och använder dessa insikter för att bland annat skapa förbättrade mekanistiska in vitro forskningsmodeller, såsom human unilocular vascularized adipocyte spheroids, HUVAS (Ioannidou et al, Journal of Physiology, 2022). Teamet studerar också effekten av olika näringsämnen på fettvävnadstillväxt, och i ett projekt lett av professor Rachel Fisher, studeras rollen av det perivaskulära fettet, som återfinns runt större blodkärl, som bidragande faktor till utvecklingen av hjärt- och kärlsjukdomar.
Inom Hagberg-teamet återfinns även en studie, ledd av Ferdinand Van T Hooft, som fokuserar på att karakterisera nya proteiner involverade i lipidmetabolismen i levern och blodcirkulationen, och deras relation till kända riskfaktorer för både metabola och kardiovaskulära sjukdomar.
Slutligen fokuserar professor Ewa Ehrenborgs team sin forskning på samspelet mellan lipidhantering, inflammation och autofag i relation till hjärt- och kärlsjukdom. Specifikt handlar deras intressen kring hur lipidhanteringen i makrofager påverkar inflammation och autofagi (lipidnedbrytning) under åderförkalkningsprocessen, något som i stort sett har förblivit okänt. De syftar också till att identifiera faktorer/proteiner i autofagiprocessen som är av relevans för progression av åderförkalkning i kärlväggen.
Tillsammans täcker dessa kombinerade forskningslinjer ett brett spektrum av organ och mekanistiska studier av mänsklig kardiometabol patofysiologi, och syftar till att förstå vad som främjar uppkomsten av sjukdom vid fetma och åldrande, och hur vi kan utveckla nya terapeutiska verktyg för att minska sjukdomsbördan.

