På väg mot friskare lungor
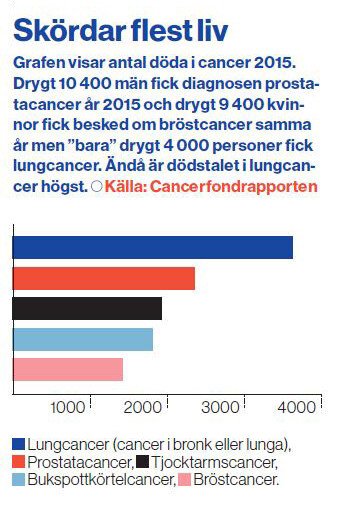
Lungcancer är den femte vanligaste cancerformen i Sverige och drabbar årligen långt under hälften så många som drabbas av prostatacancer eller bröstcancer, som ligger i topp. Trots det är lungcancer den cancerform som dödar ojämförligt flest svenskar varje år.

Text: Fredrik Hedlund, först publicerad i tidningen Medicinsk Vetenskap nr 1/2018
DET BEROR PÅ att prognosen är så dålig. Drygt 4 000 personer fick diagnosen lungcancer år 2015, medan dödstalet i lungcancer samma år landade på strax över 3 600 personer (att jämföra med cirka 2 350 döda i prostatacancer och drygt 1 400 döda i bröstcancer). I snitt lever bara hälften av de som får en lungcancerdiagnos ett år senare och femårsöverlevnaden är så låg som 15 procent.
Det främsta skälet till den dåliga prognosen för sjukdomen är att den ofta upptäcks för sent när tumören i lungan redan har utvecklat sig och börjat avge metastaser, dottersvulster runt om i kroppen. Medelåldern vid diagnos ligger runt 70 år, men lungcancer drabbar även yngre personer. 2015 var det cirka 90 personer yngre än 50 år som fick en lungcancerdiagnos.
Efter att under lång tid ha varit en sjukdom som övervägande drabbat män har könsfördelningen förändrats under de senaste åren. Åren 2012 och 2013 var den åldersstandardiserade risken lika för män och för kvinnor och sedan dess har lungcancer blivit vanligare bland kvinnor än bland män. Redan 2005 passerade lungcancer bröstcancer som den cancerform som dödar flest kvinnor i Sverige.
Lungcancer är tätt kopplad till rökning och 85-90 procent av alla som får diagnosen är rökare eller före detta rökare. Något som också har skapat ett stigma kring sjukdomen där de drabbade inte sällan förebrår sig själva för att de har drabbats samtidigt som det tidigare har varit svårt att få loss forskningsmedel till lungcancerforskning. Något som nu håller på att ändras.
Rökvanor 30-40 år tillbaka i tiden
Skillnaderna mellan könen i diagnosutvecklingen speglas också mycket av rökvanorna i befolkningen 30-40 år tillbaka. Bland män var rökning som vanligast på 1960-talet då cirka hälften av alla män rökte. Kvinnornas topp inträffade istället under 1980-talet då ungefär var tredje kvinna rökte. Andelen rökare minskade tidigare bland männen vilket nu ses i lungcancerstatistiken. Men totalantalet män i Sverige som får diagnosen har inte gått ned trots att allt färre män röker generellt.

– Det hänger ihop med att vi lever allt längre och fler hinner få sjukdomen vilket gör att vi har haft ett ganska stabilt läge sedan 70-talet, säger Per Gustavsson, professor i yrkes- och miljömedicin vid Institutet för miljömedicin, Karolinska Institutet.
Hans forskning fokuserar på de andra riskfaktorerna för lungcancer som inte är rökning, framför allt i arbetsmiljön, men också luftföroreningar i allmän miljö. Han poängterar att lungcancer i vissa fall kan härledas till kombinationer av flera olika orsaker.
Den näst största riskfaktorn för att drabbas av lungcancer hittar vi på hemmaplan.
– Radon i bostäder bidrar till cirka 500 fall av lungcancer varje år, säger han.
Men även här är ledtiderna långa så de som får diagnosen nu utsattes för radon för 20 till 40 år sedan.
– Sedan dess har man sänkt gränserna för radonhalterna i bostadshus så med de radonhalter vi har idag är riskerna mindre, säger Per Gustavsson.
När det gäller risker i arbetsmiljön så har de främst undersökts bland män eftersom det oftast har varit män som har haft arbeten som innebär exponering för riskfaktorer för lungcancer som till exempel byggnadsarbetare, stenhuggare och gruvarbetare.
– Mellan 15 och 25 procent av lungcancerfallen bland män kan tillskrivas arbetsmiljön eftersom man skulle undvika dem om man fick bort exponeringen i arbetsmiljön. Så det är mycket, säger Per Gustavsson.
Fakta: Körtelcancer vanlig
Lungcancer delas in i flera undergrupper beroende på utseende och placering i lungorna:
- Icke småcellig lungcancer. 85 procent av alla lungcancerfall.
- Adenocarcinom. Vanligaste formen av lungcancer. Kallas också körtelcancer eftersom den växer från körtelceller i lungorna.
- Skivepitelcancer. Näst vanligaste formen av lungcancer. Börjar i luftrören.
- Småcellig lungcancer. 15 procent av alla lungcancerfall. Växer snabbt och har ofta spridit sig vid upptäckt. Drabbar nästan bara rökare.
Lungcancer delas in i fyra stadier, som bland annat tar hänsyn till tumörstorlek, om lymfsystemet är påverkat och om cancern har spridit sig:
- Stadium I. En begränsad tumör som inte spridit sig utanför lungan eller luftrören.
- Stadium II och III. Cancerceller finns i en eller flera lymfkörtlar.
- Stadium IV. Cancern är spridd med metastaser i andra organ.
Den sannolikt mest välkända arbetsmiljörisken som orsakar lungcancer är asbest vars fibrer sätter sig i lungorna och orsakar utveckling av tumörer, bland flera andra hälsorisker. Att materialet var ohälsosamt upptäcktes redan under första delen av 1900-talet, men först 1982 förbjöds användandet av asbest i Sverige. Men det innebär inte att problemet är borta. Det finns fortfarande kvar i de byggnader där det användes före förbudet. Byggnader som nu börjar renoveras. Då gäller det att de ansvariga för renoveringen har koll på om asbest finns, vilket inte alltid verkar vara fallet, menar Per Gustavsson.
– Exempelvis när man ska göra stambyten på hus från 1950 – 60-talen. Där kan det finnas asbest, till exempel i kakelfixet i badrummen. När man knackar loss gammalt kakel så kan byggnadsarbetarna utsättas för asbest. För varje nytt hus måste man ta prover och skicka på analys för att se om det finns asbest eller inte – finns det asbest är det särskilda skyddsregler som gäller – och det gör man kanske inte alltid. Patienter och folk i byggbranschen ger i alla fall den bilden, säger Per Gustavsson.
Riskfaktorer som inte har eliminerats
Att asbest, 35 år efter förbudet, fortfarande är den främsta arbetsmiljörelaterade orsaken till lungcancer visar hur långsamt preventiva åtgärder får effekt på utvecklingen av lungcancer. Men det finns också riskfaktorer som inte har eliminerats från arbetsplatser och allmän miljö. Den viktigaste av dem är stendamm eller kvarts som i yrkeslivet kan hittas inom byggindustrin, vid stenbearbetning och vid tunnelbyggnationer till exempel.
– Inom yrkeslivet är det en exponering som man verkligen skulle behöva sänka. Arbetsmiljöverket har föreslagit en sänkning av dagens gränsvärde till hälften, men intressen bland arbetsmarknadens parter ifrågasätter detta, säger Per Gustavsson.
En annan riskfaktor som finns både i yrkeslivet och i stadsmiljön är dieselavgaser. De klassades som cancerframkallande så sent som 2012. Men trots det är det lite oklart hur farliga de faktiskt är idag. De fall av lungcancer orsakade av dieselavgaser som läkarna ser nu beror på exponering för länge sedan och både dieselbränslet och motorerna har förbättrats sedan dess.
– Det tar 20-30 år att få lungcancer både av tobaksrökning och av diesel. Så när vi ser att detta är en stark cancerframkallande faktor nu så vet vi ju dock inte hur stor risken är i dieselexponerade miljöer idag, det beror på hur väl man har lyckats utveckla dieseltekniken, säger Per Gustavsson.
Något som naturligtvis har betydelse för hur oroad man bör vara för dieselavgaser i staden.
– I staden är det en kombination av gatudamm, som delvis innehåller kvarts, och avgaser från trafiken, och där har vi både diesel och bensin. Tidigare hade vi också bostadsuppvärmning när man eldade i kaminer och kakelugnar i staden som man gjorde på 1900-talet och skapade höga nivåer av luftföroreningar, säger Per Gustavsson.
Enligt den senaste Miljöhälsorapporten från Folkhälsomyndigheten och Karolinska Institutet från 2017 beräknas medellivslängden i Sverige förkortas med i genomsnitt sex månader på grund av luftföroreningar, mer i söder än i norr och mer i tätorter än på landsbygden. När det gäller lungcancer specifikt finns det en studie från år 2000 som pekar på att upp till vart tionde fall av lungcancer i Stockholm skulle kunna bero på luftföroreningar från trafiken 20 år tidigare, men uppskattningen anges som osäker.
Icke småcellig lungcancer dominerar
Lungcancer delas in i småcellig och icke småcellig där den senare är helt dominerande och utgör 85 procent av fallen. Icke småcellig lungcancer delas i sin tur in i tre undergrupper; adenocarcinom (eller körtelcancer), skivepitelcancer och storcellig lungcancer. Läkarna delar också in tumörerna i fyra olika stadier beroende på storlek och spridning (se faktaruta).
En stor anledning till den dåliga prognosen vid lungcancer är att tumörerna upptäcks för sent, när de redan har hunnit utveckla sig till de senare stadierna och då inte längre är möjliga att operera bort. Men för tumörer som upptäcks i tidiga stadier är prognosen god och en operation innan tumören spridit sig är idag ett av få sätt att bota sjukdomen. Men det håller på att ändra sig. Det senaste decenniet har kunskapen och möjligheterna att behandla lungcancer förbättrats på ett dramatiskt sätt.

– Från att ha behandlat all lungcancer på ungefär samma sätt, med cytostatika, har vi nu upptäckt att sjukdomen kan delas in i olika undergrupper beroende på vilka mutationer som finns i tumören. Och sedan har nya läkemedel tagits fram som kan gå in och blockera de här signalerna i tumörerna, ofta med väldigt bra effekt, säger Simon Ekman, överläkare vid Karolinska Universitetssjukhuset och docent vid institutionen för onkologi-patologi, Karolinska Institutet.
Läkarna tar prover på tumören och sätter in behandling på de patienter som har varianter av lungcancer med mutationer som är behandlingsbara. De nya behandlingarna är också betydligt enklare för patienterna att ta jämfört med cytostatika eftersom de intas i tablettform, hemma och de har för det mesta heller inte lika mycket biverkningar eftersom de är målinriktade på tumörcellerna.
– För livskvaliteten är det ju en tydlig vinst. Jämfört med cytostatika vinner man både livskvalitet, tumörrespons och livslängd, säger Simon Ekman.
Mutationerna som behandlingarna riktas mot ligger bara bakom cirka en femtedel av lungcancerfallen i Sverige. Ungefär 12 – 15 procent av patienterna har en mutation i en tillväxtreceptor som kallas EGFR (Epidermal Growth Factor Receptor), fyra till fem procent har en mutation som kallas ALK (Anaplastic Lymphoma Kinase) och två procent har en mutation kallad ROS1, men mycket forskning pågår för att hitta behandlingar till fler mutationer, berättar Simon Ekman.
– Så vi kan förvänta oss att det kommer att fyllas på med behandlingar mot nya undergrupper inom kort. I nuläget uppskattas att cirka 70 procent av alla lungcancerfall har en sådan här drivande mutation, säger han.
Ett bekymmer är dock att den goda effekten av de målinriktade behandlingarna inte verkar sitta i. Tumören utvecklar så småningom en typ av resistens mot behandlingen.
– Förr eller senare kan man säga att i princip alla patienter får en ökning av tumören igen. Det kan vara efter ett antal år, men det kan också ske snabbare. Och då är det en slags resistensmekanism där någon del av tumören utvecklas på ett annat sätt och undgår den blockad som man har lagt på, säger Simon Ekman.
Målinriktade behandlingar
Men då går det att ta ett nytt prov och i en del fall hitta en ny målriktad behandling att sätta in. Utvecklingen går snabbt och de målinriktade behandlingarna finns nu i flera generationer med lite olika verkningsmekanismer som har visat sig framgångsrika när tumören blir resistent mot tidigare behandling. Utvecklingen är just nu en slags kapplöpning mellan forskarna och tumörerna. Simon Ekmans egen forskning handlar bland annat om att försöka hitta de genetiska förändringar som leder till resistens och ta reda på varför den utvecklas hos patienterna. Målet är att kunna hitta nya sätt att angripa resistensutvecklingen.
Men det finns fler positiva nyheter när det gäller behandling av lungcancer. Ännu nyare än de målinriktade behandlingarna är nämligen något som kallas för immunterapi. Forskarna har funnit att tumörer ofta har ett sätt att undvika attacker från det mänskliga immunförsvaret som det går att störa. Tumörcellerna kan kapa immunförsvaret genom att binda till en receptor på några av immunförsvarets celler och därigenom neutralisera immunförsvarets möjlighet att attackera dem.
De nya läkemedlen riktar sig antingen mot receptorn på immunförsvarscellerna med det lite dramatiska namnet programmerad celldödsprotein PD-1, eller mot den programmerade dödsliganden PD-L1 som finns på cancertumörens yta. Syftet är att blockera bindningen och inte låta tumören komma undan immunförsvaret.
Läkemedlen godkändes först mot hudcancer 2014 och har minskat dödligheten i sjukdomen dramatiskt. Därefter testades de och godkändes för behandling av lungcancer.
– Detta är ju också en slags målinriktad behandling, kan man säga i och med att den riktar sig mot en särskild immunfaktor, men den är betydligt bredare eftersom man mobiliserar ganska stora delar av immunförsvaret. Även om läkemedlet är målinriktat mot en specifik faktor så utlöser det en immunologisk kedjereaktion som fungerar på en bredare grupp av patienter, säger Simon Ekman.
För vissa patienter är effekten mycket god. Beroende på vilken immunterapi som ges får mellan 20 och 45 procent av patienterna ett direkt tumörsvar där tumören krymper ihop, andra får en stabilisering av tumörens utveckling medan ytterligare andra inte får någon större effekt alls. Riktigt varför vissa tumörer svarar och andra inte vet man inte, men det pågår en intensiv forskning kring detta. Det forskas också mycket kring möjligheten att kombinera olika behandlingar.
– En viktig del i utvecklingen är att hitta kombinationer som ger ännu bättre svar än enbart singelbehandling. Det pågår en mängd olika studier med kombinationer av målriktade behandlingar och immunterapi och cytostatika. Bara inom lungcancerområdet pågår det uppemot 360 olika immunterapistudier och sett till alla tumörformer pågår över 1 800 studier så det är en enorm satsning, säger Simon Ekman.
En extra skjuts till världens cancerforskning kommer det som kan betraktas som cancerforskningens eget Nobelpris tveklöst att ge. Den framgångsrike svenske affärsmannen Bengt Sjöberg avled i januari 2017, 68 år gammal i lungcancer utan att någonsin rökt en enda cigarett. Innan han dog hade han bildat en stiftelse till vilken han donerade huvuddelen av sin förmögenhet – två miljarder kronor – för användning inom cancerforskningen. Det är den största enskilda donationen till forskning som någonsin gjorts i Sverige, till och med större än Alfred Nobels testamenterade förmögenhet som omräknat till dagens penningvärde skulle motsvara 1,7 miljarder kronor.
Likt Nobelpriset delas Sjöbergpriset ut årligen och prissumman är densamma, en miljon dollar. Det allra första Sjöbergpriset delades ut 2017 till de två amerikanska forskarna Tony Hunter och James Allison vars forskning ligger bakom utvecklingen av de målinriktade läkemedlen respektive immunterapin.
Effektivare bestrålningsmetoder
Mitt bland alla dessa nya, prisade, behandlingar har också en äldre behandlingsform en viktig roll i behandlingsarsenalen. Det är strålterapin som tekniskt har förbättrats avsevärt när det gäller precisionen, vilket både innebär effektivare bestrålningsmetoder och färre biverkningar. Dessutom har, parallellt med denna utveckling, även bildåtergivningstekniken förfinats vilket ytterligare bidrar till den ökade precisionen av strålterapin. Denna precisionsstrålterapi, även kallad stereotaktisk strålterapi, är utvecklad vid Karolinska universitetssjukhuset.

– Kliniker och fysiker på Karolinska universitetssjukhuset har varit de första i världen att visa att det var möjligt att ge stereotaktisk strålterapi som dödar tumörerna, säger Rolf Lewensohn, professor i onkologi vid institutionen för onkologi-patologi, Karolinska Institutet och överläkare vid Karolinska univeritetssjukhusets onkologiska klinik.
Det handlar om de lungcancerpatienter som upptäcks tidigt i stadium I, men som, av olika skäl, inte kan opereras.
Precisionsstrålterapin är en teknik som nu har vuxit globalt och används i hela västvärlden på de sjukhus där de avancerade strålterapianläggningar som krävs finns.
Rolf Lewensohn och hans grupp har gått vidare med strålningstekniken och håller nu på att utveckla metoder för att bestråla metastaser för att kunna behandla patienter även i senare stadium med precisionsstrålterapi.
– Vi har utvecklat möjligheter att bestråla metastaser som ligger i lever, i binjurar, i lungor och till och med i kotkroppar. Vid begränsad metastasering tror vi att vi genom sådan här bestrålning på ett väsentligt sätt kan förlänga tiden till ett återfall, alltså förlänga livet på patienten, säger han.
Studier pågår dessutom nu där precisionsstrålterapi kombineras med immunterapi, där idén är att strålterapin triggar immunsystemet, berättar Rolf Lewensohn.
– Vi vågar inte tala om bot ännu för vi måste först förstå vilka patienter som det skulle kunna gälla för. Men vad vi hoppas på är att kunna åstadkomma flera års förlängning av livet, med milda biverkningar så att det verkligen ger livskvalitet, säger han.
Majoriteten av fallen upptäcks sent
Men trots alla goda behandlingsnyheter är ett stort problem fortfarande att lungcancer i majoriteten av fallen upptäcks sent, när tumören redan har avancerat till lymfkörtlar och ibland även bildat metastaser och är svårare att behandla. Man har därför länge talat om olika metoder för att screena riskpersoner för att kunna upptäcka tumörerna tidigare. På 1980-talet gjordes screeningstudier med lungröntgen som inte kunde visa någon ökad överlevnad, 1999 kom den första studien där man istället använde lågdos-datortomografi som kunde visa bättre effektivitet i att hitta patienterna, men sedan dess har det debatterats om en screeningverksamhet verkligen skulle kunna minska dödligheten.
Ända tills 2011 då studien ”National Lung Screening Trial”, NLST, publicerades. Där hade över 53 000 amerikanska storrökare screenats i tre års tid och studien kunde visa en 20-procentigt minskad dödlighet i lungcancer. Visserligen var minskningen av den totala dödligheten bara 6,7 procent, men det räckte för att amerikanska myndigheter 2013 skulle rekommendera årlig screening av storrökare och före detta storrökare mellan 55 och 74 år.

I Europa avvaktar fortfarande de nationella myndigheterna en studie från Belgien och Nederländerna kallad Nelson, där strax under 16 000 storrökare eller före detta storrökare har lottats till screening med lågdos-datortomografi eller inte. Resultaten förväntas presenteras i år eller nästa år och är det som sannolikt kommer att avgöra om screening ska införas även i Europa.
– Om den är positiv är det nog ingen tvekan, visar den något annat får man väl fundera. Jag tror absolut att vi hamnar där till slut med någon slags screening, säger Simon Ekman.
Och hans syn backas upp av en europeisk expertgrupp på screening för lungcancer som i december 2017 publicerade ett så kallat ”EU position statement” där de rekommenderar unionens länder att börja planera för ett införande av lungcancerscreening inom fyra år.
Frågan kan verka enkel. Screena storrökare och sänk dödligheten i lungcancer med 20 procent. Men det finns en hel del faktorer att överväga. Screeningprogrammet kan i sig självt orsaka en del skada genom överdiagnostisering, onödiga utredningar och operationer av godartade tumörer, psykologiskt lidande samt den extra strålning som deltagarna utsätts för. Särskilt det psykologiska lidandet kan bli kännbart eftersom hela 96 procent av de som först misstänktes ha lungcancer visade sig vara falskt positiva, det vill säga de hade inte lungcancer, i den amerikanska studien.
– Vi kommer att upptäcka en massa prickar på lungor som behöver följas under flera år varav majoriteten aldrig utvecklas till en cancer. Det kan bli en resursfråga hur dessa ska följas och av vem, säger Simon Ekman.
I den resurskampen är det viktigt att synen på lungcancer som något självförvållat inte påverkar besluten negativt, menar Simon Ekman.
– Vi jobbar hårt för att ta bort skamstämpeln kring sjukdomen och jag upplever att den börjar minska. Det är ju också en samhällskostnad i andra ändan om folk blir sjuka, det kostar mycket att ta hand om en avancerad lungcancer. På så sätt är det en vinst att försöka hålla folk friska, säger han.
Både hitta och följa tumörer
Men det finns också andra sätt att både hitta och följa tumörer. En omfattande forskning pågår för att identifiera och utvärdera så kallade biomarkörer, proteiner eller gener som kan avslöja att en tumör finns på plats och som helst också ska kunna visa tumörens ursprung och känslighet för behandling.
De mest spektakulära framtidsvisionerna talar om att kunna hitta tumörer mycket tidigt och med stor precision genom att analysera utandningsluft eller olika kroppsvätskor.
Men just nu är målsättningen att hitta biomarkörer i blodet som kan identifiera mutationer som kan styra behandlingen och också avgöra om behandlingen har effekt eller inte.

– I blodet kan man hitta flera olika typer av biomarkörer. Det kan vara cirkulerande tumörceller, DNA från tumören eller lösryckta protein som uttrycks i tumören som har klippts av eller lösgjorts genom cellsönderfall, säger Katalin Dobra, överläkare vid Karolinska universitetssjukhuset och docent i molekylär patologi vid institutionen för laboratoriemedicin, Karolinska Institutet.
Hon letar efter nya biomarkörer både för tidig diagnostik och för att förutse svar på olika behandlingar.
– Hur tidigt en tumör kan upptäckas beror oftast på tumörbördan och hur mycket tumörceller som återfinns i cirkulationen. Därför är det ofta först när det är en ganska framskriden tumör som den går att hitta, säger hon.
Bland annat på grund av detta jobbar forskarna med att identifiera allt fler och känsligare biomarkörer.
– I framtiden hoppas vi kunna kartlägga hela proteinprofilen, DNA-profilen eller mutationsprofilen och från det dra slutsatser om diagnostik och behandling. Det blir allt fler markörer som vi försöker kombinera. Nu har vi identifierat upp till 20 olika markörer som vi ska kombinera, säger Katalin Dobra.
I framtiden tror hon på kombinationer av ännu fler biomarkörer av olika slag. Inte minst för att kunna öka känsligheten och identifiera när tumören har utvecklat resistens mot målinriktade behandlingar och för att veta vilken behandling som då ska sättas in istället.

Samtidigt pågår det mycket forskning både på universiteten och läkemedelsindustrin för att hitta nya angreppssätt på lungcancertumörerna. En av de som söker är Kristina Viktorsson, forskare vid institutionen för onkologi-patologi vid Karolinska Institutet. Hon har studerat ett speciellt signalsystem för tillväxtfaktorer vid lungcancer och har tillsammans med sin forskargrupp upptäckt att en samling receptorer (Eph-receptorer) och ligander (Efriner) är aktiva vid lungcancer.
– Om man modulerar Efrin-ligandernas uttryck kan man förändra lungcancercellernas förmåga att överleva vilket indikerar att det här nätverket har en drivande funktion vid lungcancer, säger hon.
Dessutom verkar signalsystemet spela en roll vid resistensutveckling mot EGFR-behandling.
– Patienter som blir resistenta mot EGFR-behandling har bland annat visats ha en ökad signalering via Eph-receptorer, vilket indikerar att det skulle finnas någonting där även kliniskt, säger hon.
Intressant och stimulerande tid
Systemet tycks också kunna påverka tumörernas förmåga att skicka ut dottertumörer, metastaser, något som skulle kunna få stor betydelse i framtiden.
– I nuläget fokuserar vi på hur vi kan påverka systemet för att motverka resistensutveckling vid EGFR-behandling, men det är klart att den ultimata målsättningen är att kunna bromsa metastasering, säger hon.
Kristina Viktorsson har forskat inom lungcancerområdet i cirka 15 år och sett hela den utveckling som har skett med målinriktade behandlingar och immunterapi. Som molekylär cancerforskare är det en intressant och stimulerande tid att verka i, menar hon.
– Det har verkligen skett otroliga framsteg under de senaste tio åren. Lungcancer har, för vissa patienter, blivit en kronisk sjukdom istället för en dödsdom, men vi behöver veta mycket mer om den enskilde patientens tumör för att kunna individualisera behandlingen, säger hon.
